江苏省苏州市2015届高三上学期期末调研测试化学试题及答案(4)
学习频道 来源: 化学试题及答案 2025-04-02 大 中 小
(6)根据题中流程里提供的新信息,写出由(CH3)2C=CH2制备化合物
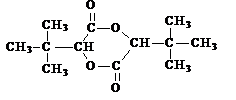
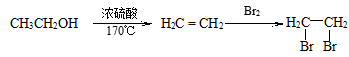 的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:
▲
18.(12分)已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]―,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍。因此,必须对含铬的废水进行处理,可采用以下两种方法。
Ⅰ.还原法 在酸性介质中用FeSO4等将+6价铬还原成+3价铬。
具体流程如下:

有关离子完全沉淀的pH如下表:
|
有关离子 |
Fe2+ |
Fe3+ |
Cr3+ |
|
完全沉淀为对应氢氧化物的pH |
9.0 |
3.2 |
5.6 |
(1)写出Cr2O2- 7与FeSO4溶液在酸性条件下反应的离子方程式 ▲ 。
(2)还原+6价铬还可选用以下的 ▲ 试剂(填序号)。
A.明矾 B.亚硫酸氢钠 C.生石灰 D.铁屑
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀。
则在操作②中可用于调节溶液pH的试剂为: ▲ (填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2 D.NaOH
此时调节溶液的pH范围在 ▲ (填序号)最佳。
A.3~4 B.6~8 C.10~11 D.12~14
Ⅱ.电解法 将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解。阳极区生成的Fe2+和Cr2O2- 7发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去。
(4)写出阴极的电极反应式 ▲ 。
(5)电解法中加入氯化钠的作用是: ▲ 。
19.(15分)CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值的化学品是目前的研究方向。
(1)已知:CH4(g) + 2O2(g)=CO2(g) + 2H2O(g) ΔH1 = a kJ•mol-1
CO(g) + H2O (g)=CO2(g) + H2 (g) ΔH2 = b kJ•mol-1
2CO(g) + O2(g)=2CO2(g) ΔH3 = c kJ•mol-1
 反应CO2(g) + CH4(g) 2CO(g) + 2H2(g) 的ΔH= ▲ kJ•mol-1。
反应CO2(g) + CH4(g) 2CO(g) + 2H2(g) 的ΔH= ▲ kJ•mol-1。
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
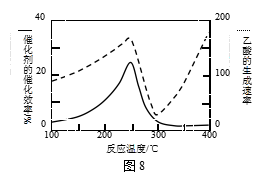 ① 在不同温度下催化剂的催化效率与乙酸的生成速率如图8所示。250~300℃时,温度升高而乙酸的生成速率降低的原因
① 在不同温度下催化剂的催化效率与乙酸的生成速率如图8所示。250~300℃时,温度升高而乙酸的生成速率降低的原因
是 ▲ 。
② 为了提高该反应中CH4的转化率,可以
采取的措施是 ▲ 。
③ 将Cu2Al2O4溶解在稀硝酸中的离子方程
式为 ▲ 。
(3)以CO2为原料可以合成多种物质。
① 利用FeO吸收CO2的化学方程式为:6 FeO + CO2=2Fe3O4 + C,则反应中每
生成1 mol Fe3O4,转移电子的物质的量为 ▲ mol。
② 以氢氧化钾水溶液作电解质进行电解,在铜电极上CO2可转化为CH4,另一
电极石墨连接电源的 ▲ 极,则该电解反应的化学方程式为 ▲ 。
20.(14分)我国某地利用生产磷铵排放的废渣磷石膏制取硫酸并联产水泥的技术研究获得成功。具体生产流程如下:
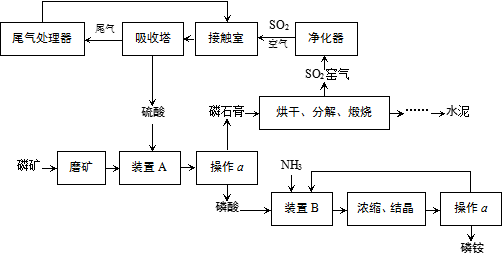
(1)操作a的名称是 ▲ 。制硫酸工艺中净化SO2窑气的目的是
▲ 。
(2)装置B中生成两种酸式盐,它们的化学式分别是 ▲ 。
(3)制硫酸所产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。能用于测定硫酸尾气中SO2含量的是 ▲ 。(选填字母)
A.NaOH溶液、酚酞试液 B.氨水、酚酞试液
C.碘水、淀粉溶液 D.KMnO4溶液、稀H2SO4液
(4)SO2可转化为硫酸盐。现有一种硫酸盐的化学式为Fe2(SO4)3·x(NH4)2SO4·yH2O。现称取该复盐2.410g,加入过量的NaOH溶液并加热,生成的气体用100mL 0.0500 mol·L―1硫酸吸收,多余的硫酸用0.2000 mol·L―1的NaOH溶液滴定,消耗NaOH溶液25.00mL。再将等质量的复盐溶于水配成溶液,加足量BaCl2溶液,充分反应后,过滤、洗涤、干燥,最后得白色沉淀2.330g。试列出计算过程确定该复盐的化学式。
▲
21.(12分)物质结构选修模块题
 (1)已知:常压下,氨气在300℃时约有9.7%分解,水蒸气在2000℃时约有4%分解,氟化氢气体在3000℃时仍不分解。这三种分子的中心原子与氢原子形成的σ键能由大到小的顺序是 ▲ ;其中水分子里的氧原子轨道的杂化类型是 ▲ 。将过量氨气通入0.1 mol·L―1的蓝色硫酸铜溶液中逐渐形成深蓝色溶液,其离子方程式为: ▲ 。
(1)已知:常压下,氨气在300℃时约有9.7%分解,水蒸气在2000℃时约有4%分解,氟化氢气体在3000℃时仍不分解。这三种分子的中心原子与氢原子形成的σ键能由大到小的顺序是 ▲ ;其中水分子里的氧原子轨道的杂化类型是 ▲ 。将过量氨气通入0.1 mol·L―1的蓝色硫酸铜溶液中逐渐形成深蓝色溶液,其离子方程式为: ▲ 。
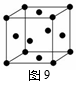
(2)用钛锰储氢合金储氢,与高压氢气钢瓶相比,具有重量轻、
体积小的优点。图9是金属钛的面心立方结构晶胞示意图,
则钛晶体的1个晶胞中钛原子数为 ▲ ,钛原子的配位数为 ▲ 。
(3)晶体硅、锗是良好的半导体材料。磷化铝、砷化镓也是重要的半导体材料,从物质结构的角度分析它们与晶体硅的关系为 ▲ 。试以原子实的形式写出31号半导体元素镓的电子排布式 ▲ 。镓与砷相比较,第一电离能更大的是 ▲ (用元素符号表示)。
化学学习经验 http://www.yggk.net/huaxue/